CRM197
다수의 항원들은 단백질에 화학적으로
연결되지 않은 한, 특히 영유아에서 면역원성이 낮아 접합체 또는 접합 백신으로 제조하여 사용한다.
CRM197은 유전자 수준에서 무독성화되었고, 접합시 장점으로 작용하는 라이신들로 이루어진 큰 보체를 보유하고 있다.
또한, 파상풍 톡소이드와 비교해 운반체-유발성 면역 반응 억제가 거의 없음을 보여주는 연구결과도 존재한다.
불용성봉입체로부터 활성 단백질을 고효율로 회수할 수 있는 자체기술을 개발하였고 이를 통해 재조합 CRM197을 대장균에서 높은 수율로 정제하는 데 성공하였다. 기존 다당류 백신의 보조제 용도 이외의
뇌종양 의약품 및 치매치료제에 접합하여 뇌세포에 쉽게 전달될 수 있는 추가적인 응용 연구를 수행하고 있다.
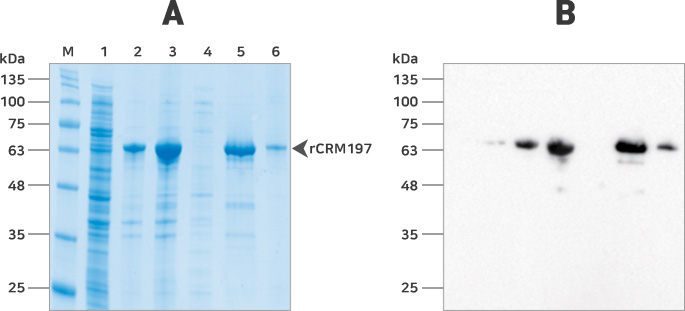
Fig. Purification of CRM197 solubilized from inclusion bodies. (A) SDS-PAGE analysis of each protein sample from each processing step. The dilution ratio of the insoluble fraction (lane 2) was the same as that of the soluble fraction (lane 1). (B) Western blot analysis of each protein sample fraction from each processing step. After transferring proteins into PVDF membrane, signal was detected signal using anti-DT antibody. M: molecular marker; lane 1, soluble fraction; lane 2, insoluble fraction; lane 3, proteins solubilized from inclusion bodies for loading Histrap column; lane 4, flow through fraction (His-trap column); lane 5, pooled elution fractions (Histrap column); lane 6, rCRM197 purified by size exclusion chromatography
CRM197 개발 진행 상황